
|
Zadanie 4.
Badania związane z opracowaniem technologii produkcji nowej generacji suplementów diety na bazie fosfolipidów żółtka.
Kierownik
Prof. Czesław Wawrzeńczyk
Zespół
dr Anna Chojnacka, mgr Andrzej Draus, dr Witold Gładkowski, dr Grzegorz Kiełbowicz, mgr Paweł Mituła, mgr Natalia Niezgoda, mgr Barbara Tubek, dr Damian Smuga, dr Małgorzata Smuga.

Badania realizowano w dwóch obszarach:
- Opracowania nowych metod izolowania i modyfikacji fosfolipidów z żółtka jaja kurzego. (Modyfikacje obejmowały zarówno część acylową jak i polarną cząsteczki).
- Badania nad pochodnymi lecytyny z resztami acylowymi kwasów izoprenoidowych o potencjalnej aktywności antynowotworowej.
W toku badań w pierwszym z wymienionych obszarów opracowano wydajną metodę frakcjonowania lipidów żółtka, prowadzącą do uzyskania frakcji fosfolipidowej o bardzo wysokiej czystości (100% w skali laboratoryjnej). Metoda wykorzystuje malejącą, wraz z obniżaniem temperatury, rozpuszczalność fosfolipidów w acetonie, a kluczowym etapem jest precypitacja uzyskanego w wyniku ekstrakcji etanolem osadu fosfolipidów w układzie heksan-aceton. Uzyskana frakcja fosfolipidowa jest pozbawiona całkowicie triacylogliceroli oraz cholesterolu, co jest niezwykle pożądane w kontekście zastosowania fosfolipidów jako suplementów diety. Dodatkową zaletą opracowanej metody jest brak konieczności przeprowadzania czasochłonnej chromatografii kolumnowej.
Modyfikacje części acylowej fosfolipidów prowadzone były głównie pod kątem ich enzymatycznego wzbogacenia w wielonienasycone kwasy tłuszczowe z rodziny WNKT na drodze transestryfikacji. Skala dotychczasowych badań w tym obszarze ograniczona była wysokimi kosztami syntetycznych kwasów i ich estrów, stosowanych najczęściej w modyfikacjach fosfolipidów jako donory grup acylowych. W projekcie wykorzystano do tego celu surowce bioodnawialne – tanie, szeroko dostępne oleje roślinne, zawierające triacyloglicerole pożądanych kwasów tłuszczowych, takie jak: olej krokoszowy – źródło kwasu linolowego, olej lniany – źródło kwasu α-linolenowego, czy olej z wiesiołka, zawierający kwas linolowy oraz γ-linolenowy.
Dotychczasowe wyniki badań nad transestryfikacją fosfatydylocholiny olejami roślinnymi okazały się niezwykle interesujące. Stosując olej lniany jako dawcę grupy acylowej w obecności lipazy z Candida antarctica udało się uzyskać 23% stopień inkorporacji kwasu α-linolenowego do fosfolipidu. Wynik ten jest porównywalny ze stopniem inkorporacji tego kwasu, uzyskanym w reakcjach acydolizy fosfatydylocholiny komercyjnie dostępnym preparatem kwasu α-linolenowego. Stosując z kolei, w reakcjach enzymatycznej modyfikacji, olej z wiesiołka, osiągnięto w fosfatydylocholinie 47% zawartość kwasu linolowego (wzrost o 35% w porównaniu z wyjściowym substratem) i 4% zawartość kwasu γ-linolenowego.
Cennym osiągnięciem było opracowanie nowej metody analizy pozycyjnej kwasów tłuszczowych w fosfolipidach, opartej na jednoetapowej reakcji enzymatycznej z udziałem lipazy z Mucor miehei. Metoda umożliwia poznanie profilu kwasów tłuszczowych w obydwu pozycjach szkieletu glicerolowego, a jej zaletą jest łatwość i szybkość jej wykonania. Z tego względu może znaleźć szerokie zastosowanie w badaniach struktury fosfolipidów. Ponadto opracowano nową, wysoce powtarzalną metodę analizy produktów hydrolizy lecytyny z wykorzystaniem chromatografii cieczowej (HPLC). Metoda ta znajdzie zastosowanie w monitorowaniu stopnia czystości otrzymanych, modyfikowanych fosfolipidów.

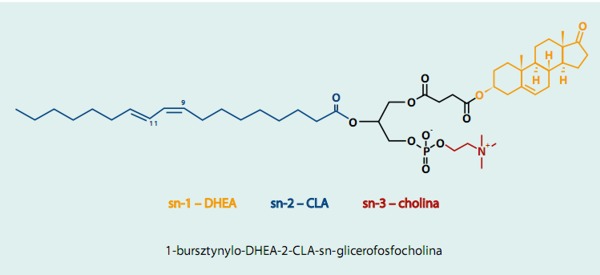
W ramach modyfikacji części polarnej fosfolipidów otrzymano pochodne fosfolipidowe z wbudowanymi, biologicznie aktywnymi związkami, takimi jak dehydroepiandrosteron (DHEA) i jego 7α-hydroksylowa pochodna oraz należąca do triterpenów betulina. Uzyskane modyfikaty będą służyły jako potencjalne nośniki wymienionych farmaceutyków o aktywności neuroprotekcyjnej, cytotoksycznej, przeciwzapalnej, antydrobnoustrojowej, ułatwiające ich przenikanie przez błony komórkowe do wnętrza docelowych komórek.
| Projekt współfinansowany ze środków Europejskiego Funduszu Rozwoju Regionalnego. | Kontakt |